H2S: Hydro Sunfua, còn được gọi là hydrogen sulfide (H₂S), là một hợp chất hóa học bao gồm 2 nguyên tử hydro và 1 nguyên tử lưu huỳnh.
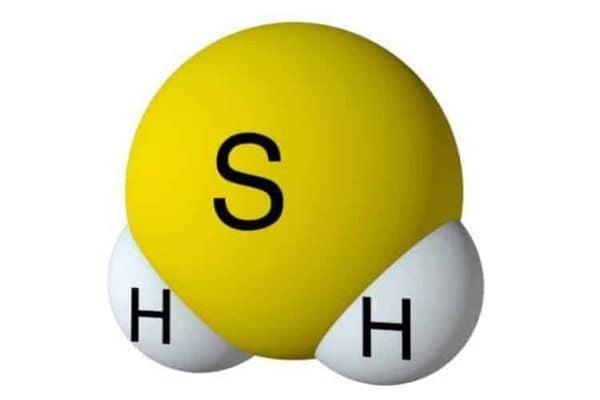
Công thức phân tử khí H2S, ảnh sưu tầm
Giải thích công thức H2S
- H biểu thị nguyên tố Hydro.
- 2 là số nguyên tử Hydro trong mỗi phân tử H2S.
- S biểu thị nguyên tố Lưu huỳnh.
- 1 là số nguyên tử Lưu huỳnh trong mỗi phân tử H2S.
Cấu trúc phân tử H2S
- Phân tử H2S có cấu trúc góc, với nguyên tử Lưu huỳnh ở vị trí trung tâm và hai nguyên tử Hydro liên kết với nó bằng liên kết cộng hóa trị.
- Góc liên kết H-S-H xấp xỉ 92 độ.
- Chiều dài liên kết H-S là 133,9 pm.
Đây là một chất khí không màu, có mùi trứng thối đặc trưng và rất độc hại. Dưới đây là một số đặc điểm và ứng dụng của hydrogen sulfide:
Tính chất hóa học của hydrogen sulfide H2S
Tính axit yếu
H₂S trong nước tạo thành dung dịch axit yếu:
H2S → H+ + HS−
HS− → H+ + S2−
Phản ứng với kim loại
H₂S phản ứng với nhiều kim loại, đặc biệt là những kim loại ít hoạt động hơn như bạc (Ag), thủy ngân (Hg) để tạo thành muối sunfua kim loại:
H2S + Ag → Ag2S + H2
Phản ứng với bazơ
H₂S phản ứng với dung dịch bazơ để tạo thành muối sunfua và nước:
H2S + 2NaOH → Na2S + 2H2O
Phản ứng oxi hóa – khử
H₂S dễ dàng bị oxi hóa thành lưu huỳnh tự do (S) hoặc axit sunfuric (H₂SO₄) tùy theo điều kiện:
2H2S + O2 → 2S + 2H2O
2H2S + O2 → 2S + 2H2O
H2S + 4HNO3 → H2SO4 + 4NO2 + 2H2O
H₂SO₄ được đọc là “axit sun-fu-ric” hoặc “axít sul-fu-ric”
Phản ứng với ion kim loại nặng
Xem thêm : Muối natri phenolat phản ứng với dung dịch HCl thu được phenol
H₂S phản ứng với dung dịch muối của kim loại nặng để tạo thành kết tủa sunfua kim loại:
H2S + CuSO4 → CuS + H2SO4
CuS được đọc là “đồng (II) sunfua”
CuSO₄ được đọc là “đồng (II) sunfat” hoặc “đồng (II) sunphat”
Phản ứng cháy
H₂S có thể cháy trong không khí, tạo thành lưu huỳnh dioxide (SO₂) và nước:
2H2S + 3O2 → 2SO2 + 2H2O
Những tính chất này làm cho H₂S là một chất hóa học có tính ứng dụng rộng rãi nhưng cũng nguy hiểm do tính độc và khả năng gây ăn mòn.
Tính chất vật lý của Hydro sulfide (H₂S)
- Trạng thái:Ở nhiệt độ phòng, H₂S là một chất khí không màu.
- Mùi: H₂S có mùi trứng thối đặc trưng và rất mạnh, dễ nhận biết, ngay cả ở nồng độ rất thấp.
- Độ tan trong nước:H₂S tan tốt trong nước, tạo thành dung dịch axit yếu (axit hydro sunfuric).
- Tỉ trọng: Khí H₂S nặng hơn không khí (khối lượng mol của H₂S là khoảng 34 g/mol so với không khí là khoảng 29 g/mol).
- Nhiệt độ sôi:Nhiệt độ sôi của H₂S là -60.28°C (-76.50°F).
- Nhiệt độ nóng chảy:Nhiệt độ nóng chảy của H₂S là -85.5°C (-121.9°F).
- Khả năng ăn mòn:H₂S là một chất ăn mòn và có thể gây hại cho kim loại và một số vật liệu khác khi tiếp xúc trong thời gian dài.
- Độ độc: H₂S rất độc và có thể gây nguy hiểm cho sức khỏe con người nếu hít phải với nồng độ cao.
Những tính chất vật lý này làm cho H₂S là một chất khí dễ bay hơi, dễ nhận biết qua mùi và cần được xử lý cẩn thận do tính độc và khả năng ăn mòn của nó.
Đặc điểm của hydrogen sulfide (H2S) trong đời sống
- Mùi đặc trưng: H₂S có mùi trứng thối đặc trưng, dễ nhận biết ngay cả ở nồng độ rất thấp.
- Độc tính cao: Khí này rất độc, có thể gây ngạt thở chết người, động vật nếu hít phải ở nồng độ cao.
- Dễ cháy: H₂S là một khí dễ cháy, có thể tạo thành hỗn hợp nổ với không khí.
- Tính hóa học: H2S nhẹ hơn không khí, tan ít trong nước, là axit yếu.
Nồng độ khí H2S và mức độ độc của hydrogen sulfide
Ứng dụng của hydrogen sulfide (H2S)
H2S ứng dụng trong công nghiệp hóa chất
Được sử dụng trong sản xuất lưu huỳnh và các hợp chất lưu huỳnh khác, như Lưu huỳnh trioxit (SO₃), Axit sunfuric (H₂SO₄), Natrisunfat (Na₂SO₄), Kẽm sunfua (ZnS), Đồng (II) sunfat (CuSO₄),
-
Sản xuất axit sulfuric: H2S là một nguyên liệu quan trọng trong quá trình sản xuất axit sulfuric (H2SO4), một trong những hóa chất công nghiệp quan trọng nhất.
-
Sản xuất nguyên tố lưu huỳnh: H2S có thể được chuyển đổi thành lưu huỳnh nguyên tố (S), một chất quan trọng trong nhiều ngành công nghiệp.
-
Sản xuất các hợp chất lưu huỳnh khác: H2S được sử dụng để sản xuất các hợp chất lưu huỳnh khác như natri hydrosulfide (NaHS), natri sulfide (Na2S), và các hợp chất hữu cơ chứa lưu huỳnh.
-
Thu hồi kim loại: H2S được sử dụng trong quá trình thu hồi một số kim loại như đồng, niken và coban từ quặng của chúng.
Công nghiệp dầu khí
- H₂S có mặt tự nhiên trong khí thiên nhiên và dầu mỏ. Trong quá trình khai thác và xử lý dầu khí, H₂S được loại bỏ và xử lý để ngăn ngừa sự ăn mòn của thiết bị và đảm bảo an toàn.
Chất thử trong phòng thí nghiệm
Dùng để nhận biết sự có mặt của các ion kim loại trong các dung dịch thông qua phản ứng tạo thành các kết tủa sunfua kim loại.
Nghiên cứu y sinh học
H2S đóng vai trò là một phân tử tín hiệu quan trọng trong cơ thể sinh vật. Nó tham gia vào nhiều quá trình sinh lý như điều hòa huyết áp, bảo vệ thần kinh và chống viêm.
Nghiên cứu môi trường
H2S là một chất gây ô nhiễm không khí và nước. Vì vậy, việc nghiên cứu H2S giúp hiểu rõ hơn về tác động của nó đối với môi trường và sức khỏe con người.
Nông nghiệp
H2S được sử dụng trong một số loại thuốc trừ sâu.
H₂S có thể được sử dụng như một chất trung gian trong quá trình tổng hợp các hợp chất hữu cơ có hoạt tính trừ sâu và diệt nấm
Công nghiệp giấy
H2S được sử dụng trong quá trình sản xuất giấy kraft, H₂S có thể được sử dụng để làm chất tẩy trắng bột giấy.
Sản xuất nước nặng
H2S được sử dụng trong một số nhà máy điện hạt nhân để sản xuất nước nặng (D2O).
Sản xuất và điều chế H2S
Phương pháp phản ứng hóa học
Phản ứng giữa muối sunfua và axit mạnh
FeS + 2HCl → FeCl2 + H2S
Đây là phương pháp sử dụng phản ứng giữa muối sunfua (thường là sắt(II) sunfua) và axit mạnh như axit clohydric.
Phương pháp chiết xuất từ khí tự nhiên và dầu mỏ
- Khử lưu huỳnh khí tự nhiên: H₂S thường có mặt trong khí tự nhiên và dầu mỏ, được tách ra trong quá trình làm sạch khí và lọc dầu.
- Quá trình Claus: Đây là một quy trình quan trọng trong công nghiệp dầu khí, trong đó H₂S được oxi hóa một phần để tạo ra lưu huỳnh nguyên tố.
Phương pháp tổng hợp trực tiếp
Phản ứng giữa hydro và lưu huỳnh
H2 + S → H2S
Ở nhiệt độ cao, hydro có thể phản ứng trực tiếp với lưu huỳnh để tạo ra H₂S.
Phương pháp sinh học
Xử lý khí sinh học: Khí sinh học từ các quá trình phân hủy sinh học (ví dụ, từ bãi rác, hầm biogas) có chứa H₂S, có thể được tách ra qua các quá trình làm sạch khí.
Phương pháp phân hủy nhiệt
Phân hủy chất hữu cơ chứa lưu huỳnh: Một số chất hữu cơ chứa lưu huỳnh khi bị phân hủy bởi vi sinh vật hoặc nhiệt độ cao có thể giải phóng H₂S.
Ngoài ra, các quá trình tự nhiên có thể làm phát trinh H2S:
-
Quá trình phân hủy hữu cơ: Khí H2S thường hình thành trong quá trình phân hủy các chất hữu cơ, đặc biệt là trong môi trường thiếu oxy. Các hiện tượng như phân giải các chất hữu cơ, sự phân tách của các cơ thểđộng vật và thực vật, và hoạt động của vi khuẩn kỵ khí đều có thể tạo ra H2S.
-
Hoạt động núi lửa: Núi lửa cũng là một nguồn tự nhiên sản sinh H2S. Trong khí núi lửa thường chứa một lượng đáng kể H2S, được giải phóng vào khí quyển trong quá trình phun trào.
-
Nguồn địa nhiệt: Các nguồn địa nhiệt như suối nước nóng và mạch nước phun cũng có thể chứa H2S.
Xử lý H2S trong nước
Loại bỏ H₂S trong nước
-
Quá trình làm thoáng khí: Oxy hóa H₂S thành sunfat hoặc lưu huỳnh tự do bằng cách sử dụng không khí hoặc oxy.
-
Sử dụng hóa chất: Sử dụng các hóa chất như clorin, kali permanganat (KMnO₄), hoặc peroxit (H₂O₂) để oxi hóa H₂S.
-
Sử dụng than hoạt tính: Hấp thụ H₂S bằng than hoạt tính.
Quá trình sinh học
- Xử lý bằng vi sinh vật: Một số vi khuẩn có khả năng oxy hóa H₂S thành lưu huỳnh hoặc sunfat trong các hệ thống xử lý sinh học như bể bùn hoạt tính hoặc các bể lọc sinh học.
- Sử dụng vi sinh để làm sách các chất, bùn bã hữu cơ là giải pháp thường thấy trong việc làm sạch và bảo vệ môi trường nước. Đặc biệt là nước trong các ao nuôi trồng thủy sản.
Loại bỏ khí H₂S qua Quá trình hấp thụ khí
-
Quá trình hấp thụ khí H₂S thường dựa trên việc tiếp xúc giữa dòng khí chứa H₂S và một chất lỏng hấp thụ (thường là dung dịch kiềm hoặc dung dịch chứa các hợp chất hóa học có khả năng phản ứng với H₂S).
Lưu ý an toàn:Vì tính độc hại và khả năng gây chết động vật, người, việc sử dụng và xử lý H₂ S cần được thực hiện cẩn thận, với các biện pháp an toàn nghiêm ngặt.Các khu vực có nguy cơ phát sinh H₂S cần được trang bị hệ thống cảnh báo và thông gió tốt để bảo vệ người làm việc.Hydrogen sulfide thường được tìm thấy trong các quá trình phân hủy của các vật chất hữu cơ dưới điều kiện yếm khí, nhất là chất protein bị thối rữa sẽ tạo H2S lớn hơn; trong bùn ao, đầm lầy, và trong một số ngành công nghiệp như khai thác dầu mỏ và sản xuất khí tự nhiên.
Nguồn: https://thuvienhaichau.edu.vn
Danh mục: Hóa