Schwefeldioxid ist eines der beiden Oxide des Schwefels. Es gehört zur Klasse der anorganischen Verbindungen und hat die Formel SO2. Ein anderer Name ist SchwefelIVoxid.
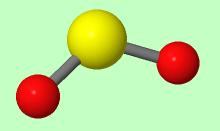
Bild 1 : Strukturformel von Schwefeldioxid
Bild 2 : SchwefeldioxidMolekül Schwefeldioxidmolekül interaktiv
Struktur
Koordination : Das Schwefeldioxidmolekül ist nicht, wie man im ersten Moment vermuten könnte, linear, sondern gewinkelt aufgebaut. Das Schwefelatom befindet sich im Zentrum, die beiden Sauerstoffatome sind an das Schwefelatom gebunden. Die beiden Bindungen bilden einen Winkel von 119,5° .
Ansehen : Starten Sie die JsmolVisualisierung durch Anklicken des Links unter dem Schwefeldioxidmolekül.
- mehr darüber, warum das Schwefeldioxidmolekül gewinkelt ist
Herstellung
Es gibt 3 Arten, wie man Schwefeldioxid herstellen kann.
Die elegante Methode
Man verbrennt Schwefel. Wer jetzt denkt, da werden in einen großen Behälter ein paar Sack Schwefel gekippt und dann angezündet, der liegt total falsch. Natürlich macht man es viel geschickter. Zuerst wird Schwefel auf etwa 150°C erhitzt. Bei dieser Temperatur ist er flüssig. Den flüssigen Schwefel sprüht man mit Hilfe von Düsen in eine Brennkammer. Er bildet dort fein verteilte Tröpfchen, die mit zugeführter Luft sowohl schnell als auch vollständig reagieren, und schon ist das Schwefeldioxid da.
Es läuft die Reaktion S + O2 → SO2 + 297 kJ ab.
Warum ist dieses Verfahren besonders elegant ? Es gibt mehrere Gründe :
- Das Ausgangsprodukt Schwefel ist in großen Mengen vorhanden. Er entsteht bei der Entschwefelung von Erdgas als Abfallprodukt, das hier eine nützliche Verwendung findet.
- Bei der Verbrennung von Schwefel entsteht nur ein einziges Produkt, nämlich Schwefeldioxid. Es entsteht nicht, wie bei vielen anderen Verfahren, ein Gemisch mehrerer Produkte, das gereinigt werden muss und aus dem man das gewünschte Produkt kostspielig und mühselig abtrennen muss.
- Flüssiger Schwefel hat bei etwa 150°C eine niedrige Viskosität. Er lässt sich dadurch leicht versprühen und bildet besonders kleine Tröpfchen. Diese haben eine große Oberfläche und verbrennen dadurch schneller.
Xem thêm : Chemikalien mit Kennzeichnung nach GHS
Zusatzinformationen
- Das Verfahren der Herstellung von Schwefeldioxid durch Verbrennung von Schwefel ist relativ neu (denn auch die Entschwefelung von Erdgas wird erst seit relativ kurzer Zeit betrieben) und wird ständig weiterentwickelt. Technische Details und neueste Entwicklungen finden Sie in mehreren Patentschriften.
- Die Verbrennung von Schwefel ist heute bei weitem das wichtigste Verfahren zur Herstellung von Schwefeldioxid.
- Gründe für die niedrige Viskosität des flüssigen Schwefels bei 150°C.
Die altertümliche Methode
Ausgangsstoffe sind schwefelhaltige Erze, in erster Linie Zinkblende, Bleiglanz und Kupferkies (sie enthalten ZnS, PbS und CuFeS2), außerdem Pyrit (FeS2). Aus diesen Erzen möchte man die Metalle Zink, Blei, Kupfer und Eisen gewinnen. Das dazu benutzte Verfahren heißt Rösten. Beim Rösten werden die zu kleinen Brocken gemahlenen Erze in spezielle Öfen gegeben, wo durch Verwirbeln, Rühren oder ähnliche Verfahren dafür gesorgt wird, dass die Erzbrocken ständig in Bewegung bleiben. Nur so kann man erreichen, dass der ganze Brocken reagiert, nicht nur die Oberfläche. Nun wird bei hoher Temperatur (etwa 650°C bis 900°C) Luft eingeblasen, und die Sulfide reagieren.
Folgende Reaktionen laufen ab : 2 ZnS + 3 O2 → 2 ZnO + 2 SO2 + 699 kJ 2 PbS + 3 O2 → 2 PbO + 2 SO2 6 CuFeS2 + 13 O2 → 3 Cu2S + 2 Fe3O4 + 9 SO2 4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2 + 3310 kJ
Welche Nachteile hat dieses Verfahren ? Es entsteht bei allen 4 Reaktionen Schwefeldioxid. Einen Haken hat die Sache aber. In der Gleichung steht als einziger gasförmiger Stoff Schwefeldioxid, und man könnte denken, aus den Öfen entweicht nichts anderes als Schwefeldioxid, vielleicht noch etwas unverbrauchte Luft. Das ist aber nicht so. Die entstehenden Gase heißen Röstgas und enthalten 2 Arten von Verunreinigungen :
- mitgerissener Staub. Er muss mit Elektrofiltern abgeschieden werden.
- Die Erze enthalten oft als Verunreinigungen Arsenverbindungen. Beim Rösten bildet sich daraus Arsentrioxid. Zur Abscheidung müssen die Röstgase auf unter 100°C abgekühlt werden, erst dann kann das Arsentrioxid mit Wasser ausgewaschen werden.
Die Herstellung von Schwefeldioxid durch Rösten ist ein umständliches, mühseliges und damit auch teures Vorhaben. Der einzige Grund, weshalb man es überhaupt macht, ist, dass das Rösten ja wegen der Metallgewinnung gemacht wird, und Schwefeldioxid als unvermeidliches Abfallprodukt sowieso anfällt.
Xem thêm : Chemikalien mit Kennzeichnung nach GHS
Zusatzinformationen
- mehr über das Rösten schwefelhaltiger Erze demnächst
- mehr über Arsentrioxid und die Frage, warum es bei so niedrigen Temperaturen entfernt werden muss demnächst
Die umweltfreundliche Methode
Bei vielen chemischen Prozessen entsteht verunreinigte Schwefelsäure. Anstatt dieses Abfallprodukt wegzuschütten, arbeitet man es auf. Dabei erhält man Schwefelsäure und Schwefeldioxid.
Bei der Herstellung von Titandioxid, dem wichtigsten weißen Farbpigment, entstehen große Mengen verdünnter und mit Eisensulfat verunreinigter Schwefelsäure, die sog. Dünnsäure. Früher hat man diese Dünnsäure ins Meer geschüttet, heute zum Glück nicht mehr. Auch beim Recycling von Dünnsäure entstehen Schwefelsäure und Schwefeldioxid.
Beide Verfahren sind energieaufwendig und teuer. Ihre Rechtfertigung erhalten sie nur durch die Vermeidung von Umweltbelastungen.
Xem thêm : Chemikalien mit Kennzeichnung nach GHS
Zusatzinformationen
- mehr über Titandioxid und seine Herstellung
- mehr über die Verklappung und das Recycling von Dünnsäure demnächst
Zum Seitenanfang
Verwendung
- Der überwiegende Teil des Schwefeldioxids wird zur Herstellung von Schwefelsäure benutzt.
Xem thêm : 1. CÓ AI THẬT SỰ QUAN TÂM (Ne 1:1-11)
Weitere Verwendungsmöglichkeiten von Schwefeldioxid sind zum Teil eher unspektakulär, aber von der Menge her bedeutend. Andere sind bekannter, spielen aber mengenmäßig nur eine kleine Rolle. Zu den ersten gehört die Herstellung einer Reihe von Zwischenprodukten der chemischen Industrie, die dann an anderer Stelle eingesetzt werden.
- Salze der Schwefligen Säure, insbesondere Natriumsulfit (Na2SO3), Natriumdisulfit (Na2S2O5) und Natriumhydrogensulfit (NaHSO3) werden in der Foto, Papier, Textil und Lederindustrie gebraucht.
- Natriumdithionit (Na2S2O4) ist ein Hilfsmittel beim Bedrucken von Textilien.
- Alkansulfonate werden in Waschmitteln und Tensiden eingesetzt.
Schwefeldioxid selbst wird zum Desinfizieren von Weinfässern und zum Haltbarmachen von Lebensmitteln benutzt. Da es giftig ist, ist sein Einsatz in diesen Bereichen umstritten.
- Kurzinfo zum Konservieren durch Schwefeln
Schwefeldioxid in der Umwelt
Schritt 1 : Wie kommt Schwefeldioxid in die Umwelt ?
Es gibt 2 Quellen, aus denen Schwefeldioxid in die Luft gelangen kann. Die eine ist natürlichen Ursprungs. Durch Vulkanausbrüche wird eine große Menge von Schwefeldioxid in die Atmosphäre gebracht. Schätzungen für den weltweiten natürlichen Ausstoß liegen zwischen 2 und 20 Millionen Tonnen pro Jahr.
Die andere Quelle ist anthropogen, d.h. vom Menschen stammend. Es ist die Verbrennung fossiler Brennstoffe, also von Kohle und Öl. Hier schätzt man, dass pro Jahr weltweit zwischen 80 und 100 Millionen Tonnen Schwefeldioxid entstehen. Das anthropogene Schwefeldioxid macht also den ganz überwiegenden Anteil am Schwefeldioxid in der Atmosphäre aus.
Schritt 2 : Was passiert mit dem Schwefeldioxid in der Atmosphäre ?
Hier gibt es mehrere Wege. Einmal kann das Schwefeldioxid durch den Regen aus der Atmosphäre ausgewaschen Werden. Das heißt, Schwefeldioxid löst sich in Regentropfen, aber auch in Nebeltröpfchen oder in den Wassertröpfchen der Wolken auf. Sobald die Tropfen auf den Boden fallen, aber auch, wenn sie auf Gebäude fallen oder von Menschen eingeatmet werden, ist das Schwefeldioxid aus der Atmosphäre entfernt. Das heißt aber nicht, dass es nun keine Wirkung mehr hat mehr dazu weiter unten. Diese Vorgänge laufen relativ schnell ab, die Verweilzeit von Schwefeldioxid in der Atmosphäre beträgt nur wenige Tage.
Andererseits kann das Schwefeldioxid zu Schwefelsäure reagieren, die dann mit dem Regen ausgewaschen wird. Neben diesem photochemischen Weg (d.h. er wird durch energiereiche Strahlung, die in diesem Fall von der Sonne kommt, ausgelöst) ist ein zweiter Weg der Schwefelsäurebildung möglich. In stark verunreinigter Luft, und besonders im Winter, wenn durch Verbrennung von Kohle und Öl viel Schwefeldioxid entsteht, sind viele Rußteilchen und schwermetallhaltige Staubteilchen in der Luft. Sie wirken als Katalysator und beschleunigen die Reaktion von Schwefeldioxid zu Schwefeltrioxid, das dann weiter zu Schwefelsäure reagiert.
Schritt 3 : Welche Wirkungen haben Schwefeldioxid und Schwefelsäure, wenn sie aus der Atmosphäre ausgewaschen werden ?
Beide sind Bestandteile des Sauren Regens. Die Auswirkungen des Sauren Regens sind im Umweltlexikon online beschrieben. Dort werden das Waldsterben und Bodenversauerung als Folgen genannt.
Andere Auswirkungen waren weit katastrophaler. Im Dezember 1952 starben bei der Londoner SmogKatastrophe etwa 12.000 Menschen. Sie wurde ausgelöst durch ein Zusammentreffen von einem besonders hohen SchwefeldioxidGehalt der Luft und einer Inversionswetterlage, die dafür sorgte, dass das Schwefeldioxid weder in höhere Luftschichten aufsteigen konnte noch vom Wind weggeweht wurde. Diese Katastrophe war des Beginn des Umdenkens im Umgang mit Luftverschmutzung.
physikalische Eigenschaften
- Schmelzpunkt : -75,5 °C
- Siedepunkt : -10.05 °C
- Dichte im flüssigen Zustand am Siedepunkt : 1,458 g/cm3
- Dichte im gasförmigen Zustand am Siedepunkt : 3,049 g/l
- Dichte bei 15 °C : 2,77 g/l
- Löslichkeit in Wasser bei 0 °C und 1 atm : 228 g/l
- Löslichkeit in Wasser bei 20 °C und 1 atm : 94 g/l
- kritische Temperatur : 157,6 °C
- kritischer Druck : 78,84 * 105 Pa (78,84 bar)
- CAS-Nr. : 7446-09-5
Infobereich
Alle Bilder dieser Seite : Lizenz CCBYSA4.0. Bildnachweis und Lizenzinfo. Text : Lizenz CCBYSA4.0. Lizenzinfo.
Zum Seitenanfang Zum Zustandsdiagramm von Kohlendioxid Zum Schwefeltrioxid Zum Kapitel Anorganische Stoffe Zum Kapitel Elemente Zum Kapitel Organische Stoffe Zur Startseite Zur Kapitelübersicht Zur Indexseite
Impressum Datenschutzerklärung
Nguồn: https://thuvienhaichau.edu.vn
Danh mục: Hóa




