- Definition: Der pH-Wert ist der negative dekadische Logarithmus der H3O+-Konzentration in einer Lösung. Er ist eine dimensionslose Größe, wird also ohne eine zugehörige Einheit angegeben.
- Formel: pH = −lg[H3O+]
- Beispiel: In reinem Wasser beträgt die Konzentration an Hydronium-Ionen 10−7mol/L. Daraus wird mittels negativem dekadischen Logarithmus der pH-Wert von 7.
- pH-Skala: 0 (stark sauer) – 7 (neutral) – 14 (stark basisch)
- Interpretation: Der pH-Wert zeigt an, ob eine Lösung sauer oder basisch ist.
Bei Zugabe einer Säure zu einer Lösung wird sie sauer (Säure überträgt ihre Protonen auf H2O-Moleküle, somit sind mehr H3O+-Ionen als OH−-Ionen vorhanden)!
Bei Zugabe einer Base zu einer Lösung wird sie basisch (Base empfängt Protonen von H2O-Molekülen, somit sind mehr OH−-Ionen als H3O+-Ionen vorhanden)!
Bạn đang xem: Säure-Basen-Haushalt
pH-Wert-Berechnung
Je nach Stärke einer Säure bzw. Base werden für die Berechnung des pH-Wertes verschiedene Formeln angewandt. Dabei werden Konzentrationsangaben im Folgenden mit c [in mmol/L] abgekürzt.
- Starke Säuren
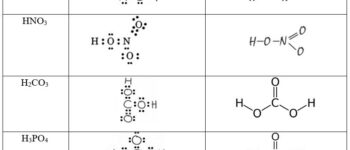
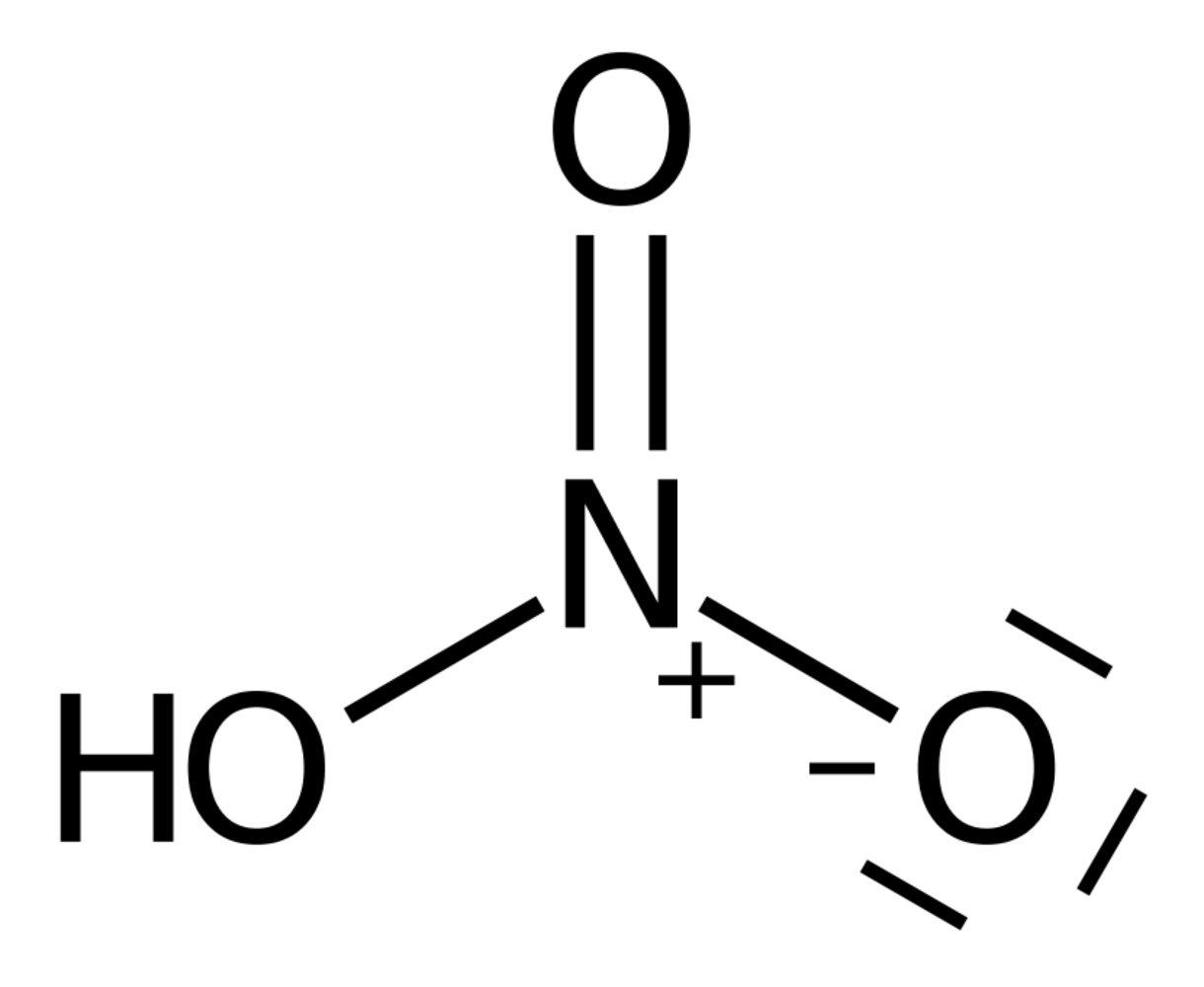
- Beispiele: Salzsäure (HCl), Schwefelsäure (H2SO4), Salpetersäure (HNO3) , Perchlorsäure (HClO4) , Trichloressigsäure (Cl3CCOOH)
- pH-Formel: pH = −lg([Säure] × Wertigkeit)
- Beispielrechnung: Wie ist der pH-Wert einer 0,05-molaren HCl-Lösung?
- pH = −lg (0,05 × 1)
- pH ≈ 1,3
- Schwache Säuren
- Beispiele: Kohlensäure (H2CO3), Zitronensäure (C6H8O7), Essigsäure (CH3COOH), Ammonium-Ion (NH4+), Phosphorsäure-Anionen (H2PO4−, HPO42−) , Propionsäure (CH3CH2COOH)
- pH-Formel: pH = ½ (pKS – lg[Säure])
- Beispielrechnung: Wie ist der pH-Wert einer 0,1-molaren Essigsäurelösung (pKS = 4,8)?
- pH = ½ (4,8 – lg(0,1))
- pH = ½ (4,8 + 1) = 2,9
- Starke Basen
- Beispiel: Hydroxid-Ion (OH−) wie z.B. in Kaliumhydroxid (KOH) und Natriumhydroxid (NaOH)
- pOH-Formel : -lg ([Base] × Wertigkeit)
- pH-Formel: pH = 14 – pOH = 14 + lg ([Base] × Wertigkeit)
- Beispielrechnung: Wie groß ist der pH-Wert einer 0,01-molaren Kaliumhydroxidlösung (KOH)?
- pH = 14 + lg (0,01 × 1)
- pH = 14 + (−2) = 12
- Schwache Basen
- Beispiele: Ammoniak (NH3), Amine
- pH-Formel: pH = 14 − ½ (pKB − lg[Base])
- Beispielrechnung: Wie groß ist der pH-Wert einer 0,1 molaren Ammoniaklösung (pKB = 4,75)?
- pH = 14 – ½ (4,75 – lg(0,1))
- pH = 14 – ½ (4,75 + 1) = 14 – 2,88 = 11,12


Autoprotolyse und der pH-Wert von Wasser
Da Wasser ein Ampholyt ist, kann ein H2O-Molekül ein Proton auf ein zweites H2O-Molekül übertragen. Das eine Wassermolekül reagiert dabei als Säure und das andere als Base. Dieser Vorgang wird auch Autoprotolyse des Wassers genannt.
- Definition
- Protolyse: Chemische Reaktion, bei der ein Proton (H+) von einem Reaktionspartner auf einen zweiten übertragen wird (Protonenübertragungsreaktion)
- Autoprotolyse des Wassers: Ein H2O-Molekül überträgt ein Proton (H+) auf ein zweites H2O-Molekül
- Reaktionsgleichung: H2O + H2O ⇄ H3O+ + OH-
- Aus dem Massenwirkungsgesetz für diese Gleichung lässt sich das sog. Ionenprodukt des Wassers berechnen (KW)
- Es gibt das Verhältnis von OH- und H3O+-Ionen in stark verdünnten Lösungen wieder
- KW= ([H3O+] × [OH−]) = 10−7 mol/L × 10−7 mol/L = 10−14 mol2/L2
- In reinem Wasser ist die Anzahl von OH- und H3O+-Ionen gleich, beide haben eine Konzentration von 10−7 mol/L (1 L Wasser enthält ca. 55 mol Wassermoleküle)
- Das Ionenprodukt des Wassers kann genutzt werden, um die pK-Werte eines korrespondierenden Säure-Basen-Paares zu berechnen: pKW = pKS + pKB = 14
- Aus dem Massenwirkungsgesetz für diese Gleichung lässt sich das sog. Ionenprodukt des Wassers berechnen (KW)
Die folgende Tabelle verdeutlicht den Zusammenhang zwischen dem Überschuss entweder von Hydronium- oder Hydroxid-Ionen in einer Lösung und dem pH-Wert:

Neutralisation und der pH-Wert von Salzlösungen
- Neutralisation: Reaktion gleicher Mengen an Säure (H+-Äquivalente) und Base (OH−-Äquivalente) miteinander, wodurch pH = 7 (neutral) erreicht wird
- Produkte: Wasser und Salz
- Beispiel: HCl + KOH ⇄ H2O + KCl
Werden Salze in Wasser gelöst, ist der pH-Wert der resultierenden Lösung nicht immer neutral (pH = 7), sondern hängt von der Säure- und Basenstärke der Ionen ab!

Rechenbeispiel (Natriumacetat):
Bei Reaktion von NaOH (= starke Base) mit Essigsäure (= schwache Säure) entsteht Natriumacetat (= ein schwach basisches Salz). Daher berechnet sich der pH-Wert über die Formel für schwache Basen:
- Gegeben sind: Konzentration Natriumacetat = 0,1mol/L und pKB (Acetat) = 9,25
- Einsetzen in die Formel (pH = 14 – ½ (pKB – lg[Base]))
- Es folgt: pH = 14 – ½ (9,25 – lg 0,1) = 14 – ½ (9,25 + 1) = 14 – 5,125 = 8,875 (schwach basischer pH-Wert)
Titration
Titration ist ein Verfahren zur experimentellen Bestimmung einer unbekannten Säure- oder Basenmenge in einer Lösung: Dazu werden exakte Mengen einer Base bzw. Säure hinzugegeben und die Veränderung des pH-Wertes mithilfe eines Indikators gemessen.
- Definition: Es gibt zwei verschiedene Formen der Titration
- Azidimetrie: Zugabe einer bekannten Menge Säure zu einer unbekannten Menge Base
- Funktion: Berechnung der Basenmenge
- Alkalimetrie: Zugabe einer bekannten Menge Base zu einer unbekannten Menge Säure
- Funktion: Berechnung der Säuremenge
- Azidimetrie: Zugabe einer bekannten Menge Säure zu einer unbekannten Menge Base
- Durchführung
- Ein passender Indikator wird ausgewählt.
- Einem Gefäß, das die zu untersuchende Säure (bzw. Base) enthält, wird tröpfchenweise das Titrationsmittel hinzugefügt.
- Der Farbumschlag zeigt das Erreichen des Äquivalenzpunktes an.
- Titrationskurve
- Erstellung
- y-Achse: Nach jeder Zugabe eines Tropfens des Titrationsmittels wird der pH-Wert gemessen und auf der y-Achse eingetragen.
- x-Achse: Die Menge des schon verbrauchten Titrationsmittels wird auf der x-Achse eingetragen.
- Besondere Kurvenpunkte
- Äquivalenzpunkt
- Definition: Hier befinden sich identische (= äquivalente) Mengen einer Säure (bzw. einer Base) und Titrationsmittel in der Lösung
- Funktion: Der Äquivalenzpunkt ermöglicht die Berechnung der gesuchten Säuremenge (bzw. Basenmenge)
- Bestimmung: Farbumschlag des Indikators, in der Titrationskurve als Punkt mit einem deutlichen pH-Sprung erkennbar (Wendepunkt im fast senkrechten Bereich)
- pH-Wert: Abhängig von der Stärke der Säure und Base
- Bei der Titration einer schwachen Säure mit einer starken Base liegt der Äquivalenzpunkt im basischen Bereich
- Bei der Titration einer schwachen Säure mit einer schwachen Base oder einer starken Säure mit einer starken Base liegt der Äquivalenzpunkt bei einem neutralen pH-Wert von 7
- Halbäquivalenzpunkt
- Definition: Titriert man schwache Säuren oder Basen, ist an diesem Punkt die Hälfte der jeweiligen Säure oder Base neutralisiert
- Bestimmung: Halbäquivalenzpunkt ablesbar am halben Titrationsvolumen des Äquivalenzpunktes
- pH: Bei schwachen Säuren oder Basen entspricht der pH-Wert am Halbäquivalenzpunkt dem pKs- bzw. pKB-Wert der Säure bzw. Base
- Neutralpunkt
- Definition: Hier ist der neutrale pH-Wert erreicht
- Funktion: Der Neutralpunkt zeigt die verbrauchte Titriermittelmenge bis Einstellung eines neutralen pH-Wertes an
- Bestimmung: pH-Messung
- pH-Wert: 7
- Äquivalenzpunkt
- Erstellung
Nguồn: https://thuvienhaichau.edu.vn
Danh mục: Hóa