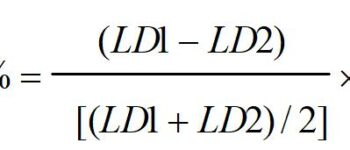FeCl2, auch Eisen(II)-chlorid genannt, ist eine chemische Verbindung mit verschiedene Eigenschaften. Es ist ein grünlich-gelber Kristall solide mit ein starker geruch. FeCl2 ist in Wasser gut löslich und bildet sich eine hellgrüne Lösung. Es ist eine paramagnetische VerbindungDas bedeutet, dass es von einem Magnetfeld angezogen wird. FeCl2 ist außerdem hygroskopisch, was bedeutet, dass es leicht Feuchtigkeit aus der Luft aufnimmt. Es wird häufig verwendet in Laboreinstellungen als Reduktionsmittel und in industrielle Anwendungen sowie Wasseraufbereitung und Farbstoffherstellung.
Key Take Away
Immobilien Beschreibung Körperlicher Status Solid Farbe Grünlich-gelb Geruch Starke Löslichkeit Gut löslich in Wasser Magnetische Eigenschaften Paramagnetische Hygroskopizität Nimmt Feuchtigkeit aus der Luft auf Gemeinsame Nutzung Reduktionsmittel, Wasseraufbereitung, Farbstoffherstellung
Bạn đang xem: Eigenschaften von Eisenchlorid (FeCl2) (25 Fakten, die Sie kennen sollten)
Identifizierung von FeCl2
FeCl2, auch Eisen(II)-chlorid genannt, ist eine anorganische Verbindung das wird häufig in verschiedenen verwendet industrielle Anwendungen. Es ist eine chemische Verbindung, bestehend aus Eisen- und Chloratome, mit chemische Formel FeCl2. FeCl2 wird identifiziert durch sein einzigartiger IUPAC-Name, also Eisen(II)-chlorid.
FeCl2 IUPAC-Name
Der IUPAC-Name denn FeCl2 ist Eisen(II)-chlorid. Dieser Name wird abgeleitet von das systematische Benennungssystem genutzt von die Internationale Union von Rein und Angewandte Chemie (IUPAC) zu standardisieren die Namen von chemischen Verbindungen.
Chemische Formel von FeCl2
Das chemische Formel von FeCl2 darstellt die Zusammensetzung Eisen(II)-chlorid. Es besteht aus ein Eisenatom (Fe). gebunden an zwei Chlor (Cl)-Atome. Das chemische Formel für FeCl2 ist FeCl2.
FeCl2 CAS-Nummer
FeCl2 wird zugeordnet ein Unikat CAS-Nummer, Das ist eine numerische Kennung Wird zur Unterscheidung chemischer Verbindungen verwendet. Das CAS-Nummer für FeCl2 ist 7758-94-3.
FeCl2 ChemSpider-ID
ChemSpider ist eine Datenbank das Informationen über chemische Verbindungen liefert, einschließlich ihre Eigenschaften und Strukturen. FeCl2 hat eine bestimmte ChemSpider-ID, Das ist eine eindeutige Kennung . die ChemSpider-Datenbank. Die ChemSpider-ID für FeCl2 beträgt 22985.
FeCl2 besitzt verschiedene physikalische und chemische Eigenschaften das macht es nützlich in verschiedene Anwendungen. Es hat ein Molekulargewicht of ca. 126.75 g/mol und eine Dichte of 3.16 g/cm³. FeCl2 ist ein grünlich-gelber Kristall bei Zimmertemperatur fest.
Hauptvorteile von die bemerkenswerten Eigenschaften von FeCl2 ist seine Löslichkeit. Es ist in Wasser, Ethanol und Aceton löslich, in jedoch unlöslich organische Lösungsmittel wie Benzol und Toluol. Dieses Löslichkeitsmerkmal ermöglicht die einfache Lösung von FeCl2 verschiedene Lösungsmittel for verschiedene Zwecke.
FeCl2 hat eine Schmelzpunkt von 677°C und a Siedepunkt von 1023 °C. Diese thermischen Eigenschaften zeigen an, dass FeCl2 standhalten kann hohe Temperaturen ohne sich zu zersetzen oder zu verdampfen, wodurch es für Anwendungen mit Hitze geeignet ist.
In Hinsicht auf seine chemische Reaktivität, FeCl2 kann durchlaufen verschiedene Reaktionen. Es kann mit Wasser unter Bildung reagieren Salzsäure und Eisen(III) Oxid. FeCl2 kann auch mit reagieren andere Metallsalze zur Bildung Doppelsalze. Diese chemische Reaktionen hervorheben die Vielseitigkeit von FeCl2 in verschiedene chemische Prozesse.
Beim Umgang mit FeCl2 ist es wichtig, Sicherheitsvorkehrungen zu treffen seine potenziellen Gefahren. FeCl2 ist ätzend und kann Haut- und Augenreizungen verursachen. Es ist auch giftig, wenn es eingenommen oder eingeatmet wird. Daher, geeignete SchutzausrüstungUm die Sicherheit zu gewährleisten, sollten beim Arbeiten mit FeCl2 Handschuhe und Schutzbrillen getragen werden.
FeCl2 kann durch Reaktion von Eisen mit Salzsäure hergestellt werden. Die Reaktion erzeugt Wasserstoffgas und FeCl2 als Ein Produkt. Das resultierende FeCl2 kann weiter gereinigt und für verschiedene Anwendungen verwendet werden.
Um FeCl2 zu speichern, wird empfohlen, es darin aufzubewahren ein dicht verschlossener Behälter weg von Feuchtigkeit und unverträgliche Substanzen. Feuchtigkeit kann dazu führen, dass FeCl2 abgebaut wird und verloren geht seine Wirksamkeit. Richtige Kennzeichnung und Lagerung in ein gut belüfteter Bereich sind unbedingt zu verhindern etwaige Unfälle oder Kontamination.
Zusammenfassend lässt sich sagen, dass es FeCl2 oder Eisen(II)-chlorid ist eine wichtige chemische Verbindung mit verschiedene Eigenschaften und Anwendungen. Sein einzigartiger IUPAC-Name, chemische Formel, CAS-Nummer und Hilfe zur ChemSpider-ID bei der Identifizierung und Kategorisierung dieser Verbindung. Verständnis die physikalischen und chemischen EigenschaftenSPACE die Sicherheitsvorkehrungen und Lagerungssansprüche, ist bei der Arbeit mit FeCl2 von entscheidender Bedeutung.
Chemische Klassifizierung von FeCl2
FeCl2, auch bekannt als Eisen(II)-chlorid, ist eine chemische Verbindung, die unter diese Kategorie fällt die Kategorie of Anorganische Verbindungen. Es ist klassifiziert als ein Chloridsalz, speziell ein Metallhalogenid. FeCl2 besteht aus Eisen (Fe) und Chlor (Cl)-Atome, Mit chemische Formel von FeCl2.
Eisen(II)-chlorid ist eine wichtige Verbindung in das Feld der Chemie aufgrund seiner verschiedene Eigenschaften und Anwendungen. Lassen Sie uns einige davon erkunden seine Hauptmerkmale und verwendet.
Eigenschaften von Eisen(II)-chlorid
FeCl2 hat eine chemische Struktur bestehend aus ein Eisenatom gebunden an zwei Chloratome. Diese Verbindung findet sich typischerweise in seine wasserfreie Form, was bedeutet, dass es nicht enthält irgendwelche Wassermoleküle. Es kann jedoch auch als existieren hydratisiert, in dem Wassermoleküle eingebaut sind seine Kristallstruktur.
Hier sind einige der physikalische Eigenschaften von FeCl2:
- Molekulargewicht: Das Molekulargewicht von FeCl2 ist ca. 126.75 g/mol.
- Dichte: FeCl2 hat eine Dichte von etwa 3.16 g/cm³.
- Schmelzpunkt: Das Schmelzpunkt von FeCl2 liegt bei etwa 677°C.
- Siedepunkt: FeCl2 hat einen Siedepunkt of ca. 1023°C.
Verwendung von Eisen(II)-chlorid
Eisen(II)-chlorid findet vielfältige Anwendungen in verschiedene Branchen. Einige seine allgemeinen Verwendungszwecke -System umfasst:
- Wasseraufbereitung: FeCl2 wird häufig als verwendet ein Gerinnungsmittel in Wasseraufbereitung Prozesse zur Entfernung von Verunreinigungen und zur Klärung von Wasser.
- Chemische Synthese: Es dient als ein Vorläufer bei der Synthese von andere Eisenverbindungen und organische Moleküle.
- Pigmentherstellung: FeCl2 wird bei der Herstellung von Pigmenten verwendet, wie z Eisenblau, das in Farben und Farbstoffen verwendet wird.
- Ätzmittel: Es wird eingesetzt als ein Ätzmittel in der Elektronikindustrie erschaffen Schaltungsmuster on Leiterplatten.
- Katalysator: FeCl2 kann als Katalysator wirken ein Katalysator in verschiedene chemische Reaktionen, fördernd die Umwandlung of eine Substanz zum anderen.
Sicherheitsvorkehrungen und Toxizität
Bei der Arbeit mit FeCl2 ist die Einnahme wichtig bestimmte Sicherheitsvorkehrungen wegen seine potenziellen Gefahren. FeCl2 kann Haut- und Augenreizungen verursachen, daher wird das Tragen empfohlen Schutzhandschuhe und Schutzbrille beim Umgang mit dieser Verbindung. Empfehlenswert ist auch das Einarbeiten ein gut belüfteter Bereich um das Einatmen zu vermeiden seine Dämpfe.
FeCl2 sollte gelagert werden ein dicht verschlossener Behälter, fern von Feuchtigkeit und unverträgliche Substanzen. Es ist wichtig, das Sicherheitsdatenblatt (MSDS) zu konsultieren spezifische Richtlinien zur Handhabung, Lagerung und Entsorgung von FeCl2.
Vorbereitung und Lagerung von FeCl2
FeCl2 kann durch Reaktion von Eisen mit Salzsäure oder durch hergestellt werden die Reduzierung of Eisen(III)chlorid. Es ist wichtig, damit umzugehen diese Reaktionen mit Vorsicht wegen die ätzende Natur of die beteiligten Chemikalien.
Bei der Lagerung von FeCl2 ist es wichtig, dass es drin bleibt eine trockene Umgebung um die Bildung von Hydraten zu verhindern. Feuchtigkeit kann dazu führen die Verschlechterung der Verbindung und des Affekts seine Eigenschaften.
Schlussfolgerung
Zusammenfassend ist FeCl2 eine anorganische Verbindung klassifiziert als ein Metallhalogenid. Es besitzt verschiedene physikalische und chemische Eigenschaften das macht es nützlich in verschiedene Anwendungen. Es ist jedoch wichtig, vorsichtig mit FeCl2 umzugehen und diese zu befolgen Sicherheitsrichtlinien sicherstellen sichere Nutzung.
Physikalische Eigenschaften von FeCl2
Eisen(II)-chlorid, auch bekannt als FeCl2, ist eine Verbindung, die Folgendes aufweist: verschiedene physikalische Eigenschaften. Sehen wir uns einige dieser Eigenschaften an Mehr Details.
Molmasse von FeCl2
Die Molmasse von FeCl2, das darstellt die Masse of ein Maulwurf der Verbindung ist ca. 126.75 Gramm pro Mol. Dieser Wert wird durch Addition berechnet die Atommassen von Eisen (Fe) und Chlor (Cl) in FeCl2.
FeCl2-Farbe
FeCl2 wird häufig als beobachtet ein hellgrüner Kristall solide. Die Farbe ergibt sich aus die Interaktion zwischen den Eisen- und Chloratome innerhalb des Geländes. Das ist erwähnenswert die Farbe von FeCl2 kann je nach variieren sein Hydratationszustand.
FeCl2-Moldichte
Die molare Dichte von FeCl2 bezieht sich auf die Masse of ein Maulwurf of die Verbindung pro Volumeneinheit. Die Berechnung erfolgt durch Division die Molmasse von FeCl2 durch sein Molvolumen. Die molare Dichte von FeCl2 ist ungefähr 3.16 gWidder pro Kubikzentimeter.
Schmelzpunkt von FeCl2
FeCl2 hat ein relativ niedriges Schmelzpunkt von rund 677 Grad Celsius. Dies bedeutet, dass bei Temperaturen darüber dieser Punkt, FeCl2 geht von einem Feststoff in einen über eine Flüssigkeit Zustand. Das Schmelzpunkt von FeCl2 kann durch Faktoren wie Verunreinigungen und die Anwesenheit von Wasser beeinflusst werden.
Siedepunkt von FeCl2
Das Siedepunkt von FeCl2 ist ca. 1023 Grad Celsius. Bei Temperaturen darüber dieser Punkt, FeCl2 unterliegt ein Phasenübergang von eine Flüssigkeit zu ein gasförmiger Zustand. Ähnlich zu Schmelzpunkt, Siedepunkt von FeCl2 kann durch Verunreinigungen und die Anwesenheit von Wasser beeinträchtigt werden.
FeCl2-Zustand bei Raumtemperatur
Bei Raumtemperatur, was normalerweise der Fall ist um die 25 Grad Celsius, FeCl2 liegt als Feststoff vor. Das bedeutet, dass es erhalten bleibt seine kristalline Struktur und ändert sich nicht ohne weiteres sein Zustand. Es ist jedoch wichtig zu beachten, dass FeCl2 Feuchtigkeit aus der Luft aufnehmen kann, was zur Bildung von führt hydratisierte Formen.
Diese physikalische Eigenschaften von FeCl2 spielen eine entscheidende Rolle in seine verschiedenen Anwendungen. Das Verständnis dieser Eigenschaften hilft bei der Bestimmung seine Eignung for spezifische Verwendungen, Wie in chemische Reaktionen, wie ein Katalysator, oder bei der Herstellung von andere Verbindungen.
Denken Sie daran, mit FeCl2 vorsichtig umzugehen, da es giftig sein kann bestimmte Sicherheitsrisiken. Es wird empfohlen, das Sicherheitsdatenblatt (MSDS) zu Rate zu ziehen genaue Information zu Handhabung, Lagerung und Sicherheitsvorkehrungen.
Zusammenfassend weist FeCl2 auf eine Molmasse of ca. 126.75 Gramm pro mol, eine hellgrüne Farbe, eine molare Dichte von herum 3.16 gWidder pro Kubikzentimeter, eine Schmelzpunkt of etwa 677 Grad Celsius, eine Siedepunkt of ca. 1023 Grad Celsius, und es liegt bei Raumtemperatur als Feststoff vor. Diese physikalische Eigenschaften beitragen zu die Gesamteigenschaften und Verhalten von FeCl2.
Chemische Eigenschaften von FeCl2
Eisen(II)-chlorid (FeCl2) ist eine chemische Verbindung, die Folgendes aufweist: verschiedene interessante chemische Eigenschaften. Lassen Sie uns einige dieser Eigenschaften im Detail untersuchen.
FeCl2 Ionische/kovalente Bindung
FeCl2 besteht hauptsächlich aus ionische Bindungen. Es besteht aus Eisen (Fe)-Kationen und Chlorid (Cl)-Anionen. Die Ionenbindung wird durch gebildet die Übertragung von Elektronen aus das Eisenatom zu die Chloratome, was zur Bildung von führt Fe2+-Kationen und Cl-Anionen. Es ist jedoch erwähnenswert, dass auch FeCl2 auftreten kann etwas kovalenten Charakter wegen das teilweise Teilen von Elektronen zwischen den Eisen- und Chloratome.
FeCl2-Ionenradius
Der Ionenradius von Fe2+ in FeCl2 ist ca. 78 Uhr. Die kleinere Größe of das Fe2+-Kation lässt es entstehen starke elektrostatische Wechselwirkungen mit die umgebenden Chloridanionen, beitragen zu die Stabilität der Verbindung.
FeCl2-Elektronenkonfigurationen
Die Elektronenkonfiguration von Fe2+ in FeCl2 ist [Ar] 3d^6. Das Eisenatom verliert zwei Elektronen von Es ist ein 4s-Orbital erreichen eine stabile Konfiguration. Diese Konfiguration ergibt Fe2+ seine charakteristischen Eigenschaften, sowie seine Fähigkeit zur Bildung Koordinationskomplexe und teilnehmen Redoxreaktionen.
FeCl2-Oxidationszustand
FeCl2 kommt hauptsächlich in vor die Oxidationsstufe +2. Das Eisenatom in FeCl2 verliert zwei Elektronen, was zur Bildung von führt Fe2+-Kationen. Allerdings unter bestimmte Bedingungen, FeCl2 kann auch oxidiert werden, um Fe3+-Ionen zu bilden.
FeCl2-Säuregehalt
FeCl2 ist eine schwache Säure und kann darin hydrolysiert werden wässrige Lösungen. Es reagiert mit Wasser unter Bildung von Salzsäure (HCl) und Eisen(III) Oxid (Fe2O3). Die Hydrolysereaktion lässt sich wie folgt darstellen:
FeCl2 + H2O → Fe2O3 + 2 HCl
Es ist wichtig, mit FeCl2 vorsichtig umzugehen und die Sicherheitsvorkehrungen zu befolgen seine saure Natur und mögliche Reaktivität.
Dies sind einige von die wichtigsten chemischen Eigenschaften von FeCl2. Bei der Arbeit mit FeCl2 in verschiedenen Anwendungen ist es wichtig, diese Eigenschaften zu berücksichtigen, z seine Anwendungen in chemische Synthese, als Reduktionsmittel oder bei der Herstellung von Pigmenten.
Sensorische Eigenschaften von FeCl2
FeCl2, auch Eisen(II)-chlorid genannt, ist eine Verbindung mit interessante sensorische Eigenschaften. Lass uns erforschen zwei Aspekte of seine sensorischen Eigenschaften: Geruch und Magnetismus.
Ist FeCl2 geruchlos?
FeCl2 ist dafür bekannt ein deutlicher Geruch. Es hat ein leicht stechender und säuerlicher Gerucherinnert an eine metallische Verbindung. Dieser Geruch kann beim Umgang oder Arbeiten mit FeCl2 festgestellt werden. Es ist jedoch wichtig, dies zu beachten die Geruchsschwelle für FeCl2 ist relativ niedrig, was bedeutet, dass es möglicherweise nicht leicht wahrnehmbar ist, es sei denn in höhere Konzentrationen or Nähe.
Ist FeCl2 paramagnetisch?
Wenn es um Magnetismus geht, weist FeCl2 auf interessante Eigenschaften. Es gilt als paramagnetisch, das heißt, es wird von einem Magnetfeld angezogen. Diese Liegenschaft entsteht durch die Anwesenheit ungepaarter Elektronen in das Fe2+-Ions innerhalb des Geländes. Diese ungepaarten Elektronen sich ausrichten ein äußeres Magnetfeld, was dazu führt, dass FeCl2 nur schwach von Magneten angezogen wird.
Zusammenfassend lässt sich sagen, dass FeCl2 ein deutlicher Geruch, als leicht scharf und säuerlich beschrieben. Es ist außerdem paramagnetisch, was bedeutet, dass es aufgrund der Anwesenheit ungepaarter Elektronen von einem Magnetfeld angezogen werden kann. Diese sensorischen Eigenschaften hinzufügen die Gesamteigenschaften von FeCl2, was es zu einer interessanten Verbindung für die Untersuchung macht.
Lassen Sie uns nun genauer darauf eingehen andere Aspekte von FeCl2, wie z seine chemische Struktur, physikalische Eigenschaften, Verwendungszwecke und mehr.
Besondere Eigenschaften von FeCl2
Eisen(II)-chlorid, auch FeCl2 genannt, besitzt mehrere besondere Eigenschaften Das macht es zu einer interessanten Verbindung zum Studieren. In In diesem Abschnitt, werden wir erkunden drei spezifische Aspekte von FeCl2: seine Hydrate, Kristallstruktursowie Polarität und Leitfähigkeit.
FeCl2-Hydrate
Xem thêm : HÓA CHẤT VIỆT QUANG
FeCl2 hat die Fähigkeit um Hydrate zu bilden, bei denen es sich um Verbindungen handelt, die Wassermoleküle in sich enthalten Kristallstruktur. Das am häufigsten vorkommende Hydrat von FeCl2 ist das Dihydrat FeCl2·2H2O. Das bedeutet, dass für jedes FeCl2-MolekülEs gibt zwei Wassermoleküle mit ihr verbundenen. Die Präsenz von Wassermolekülen erheblich beeinflussen können die physikalischen und chemischen Eigenschaften von FeCl2, wie z seine Löslichkeit, Schmelzpunkt und Siedepunkt.
FeCl2-Kristallstruktur
Das Kristallstruktur von FeCl2 ist ein wichtiges Merkmal Dies ist bei der Untersuchung dieser Verbindung zu berücksichtigen. FeCl2 übernimmt eine geschichtete Struktur, Wobei das Eisen und Chloridionen sind in abwechselnden Schichten angeordnet. Diese Anordnung entsteht die charakteristische grüne Farbe of FeCl2-Kristalledem „Vermischten Geschmack“. Seine Kristallstruktur von FeCl2 beeinflusst ebenfalls seine magnetischen Eigenschaften, wie es zeigt paramagnetisches Verhalten aufgrund der Anwesenheit ungepaarter Elektronen in die Eisenionen.
Polarität und Leitfähigkeit von FeCl2
FeCl2 ist eine polare Verbindung, was bedeutet, dass es so ist eine Trennung of positive und negative Ladungen . sein Molekül. Diese Polarität ergibt sich aus der Unterschied in der Elektronegativität zwischen Eisen- und Chloratome. Die polare Natur von FeCl2 ermöglicht es ihm, sich darin aufzulösen polare Lösungsmittel, wie zum Beispiel Wasser. Wenn sich FeCl2 in Wasser auflöst, zerfällt es in die dafür verantwortlichen Fe2+- und Cl-Ionen seine Leitfähigkeit in Lösung.
Zusammenfassend besitzt FeCl2 besondere Eigenschaften Das macht es zu einer faszinierenden Verbindung, die es zu studieren gilt. Seine Fähigkeit um Hydrate zu bilden, geschichtet Kristallstruktur, und Polarität und Leitfähigkeit tragen dazu bei seine einzigartigen Eigenschaften und Verhalten. Durch Verständnis diese Eigenschaften, können wir Einblicke gewinnen die verschiedenen Anwendungen, chemische Reaktionenund Sicherheitsvorkehrungen im Zusammenhang mit FeCl2.
Chemische Reaktionen mit FeCl2
Eisen(II)-chlorid, auch FeCl2 genannt, ist eine chemische Verbindung, die sich verändern kann verschiedene Reaktionen mit verschiedene Substanzen. Lassen Sie uns einige davon erkunden die Reaktions mit FeCl2:
FeCl2-Reaktion mit Säure
Wenn FeCl2 mit reagiert eine Säure, wie Salzsäure (HCl), eine Verdrängungsreaktion stattfindet. Das FeCl2-Molekül spendet sein Eisenion (Fe2+) zu die SäureBilden Eisenchlorid (FeCl3) und freisetzen Wasserstoffgas (H2). Die Reaktion lässt sich wie folgt darstellen:
FeCl2 + 2HCl → FeCl3 + H2
FeCl2-Reaktion mit Base
FeCl2 kann auch mit reagieren basierend, sowie Natriumhydroxid (NaOH), zu bilden Eisenhydroxid (Fe(OH)2) und Kochsalz (NaCl). Diese Reaktion is eine doppelte Verdrängungsreaktion, Wobei das Fe2+-Ion aus FeCl2 verbindet sich mit das Hydroxidion (OH-) aus die Basis. Die Reaktionsgleichung ist wie folgt:
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
FeCl2-Reaktion mit Oxid
FeCl2 kann mit reagieren eine Oxidverbindung, sowie Eisen(III) Oxid (Fe2O3), in eine Redoxreaktion. Das Fe2+-Ion aus FeCl2 wird dabei zu Fe3+-Ionen oxidiert der Sauerstoff von das Oxid ist reduziert. Diese Reaktion führt zur Bildung von Eisen(II,III) Oxid (Fe3O4) und Chlorgas (Cl2). Die ausgeglichene Gleichung for diese Reaktion ist:
3FeCl2 + Fe2O3 → 2Fe3O4 + 6Cl2
FeCl2-Reaktion mit Metall
FeCl2 kann auch mit reagieren bestimmte Metalle, wie Zink (Zn), in eine einzelne Verschiebungsreaktion. Das Fe2+-Ion aus FeCl2 ersetzt das Metall Ion in der Verbindung, sich bildend Eisenmetall (Fe) und das Chloridsalz of das Metall. Wenn beispielsweise FeCl2 mit Zink reagiert, die Reaktion kann dargestellt werden als:
FeCl2 + Zn → Fe + ZnCl2
Diese sind nur ein paar Beispiele dauert ebenfalls 3 Jahre. Das erste Jahr ist das sog. chemische Reaktionen mit FeCl2. Es ist wichtig zu beachten, dass FeCl2 mit Vorsicht gehandhabt werden sollte, da es giftig sein und Haut- und Augenreizungen verursachen kann. Richtige Sicherheitsvorkehrungen bei der Arbeit mit FeCl2 zu beachten.
Aussichten für Mehr Info on die Eigenschaften, Vorbereitung, Lagerung und Sicherheitsrichtlinien Informationen zu FeCl2 finden Sie im Materialsicherheitsdatenblatt (MSDS) von der Hersteller.
Schlussfolgerung
Zusammenfassend ist FeCl2, auch Eisen(II)-chlorid genannt, eine Verbindung mit verschiedenen interessante Eigenschaften. Es ist ein grünlich-gelber Feststoff das sich leicht in Wasser auflöst und bildet eine gelbliche Lösung. FeCl2 ist stark hygroskopisch, d. h. es nimmt leicht Feuchtigkeit aus der Luft auf. Es ist auch ein starkes Reduktionsmittel und kann mit Sauerstoff unter Bildung reagieren Eisen(III) Oxid. FeCl2 wird häufig verwendet in industrielle Anwendungen, etwa bei der Herstellung von Pigmenten, Farbstoffen usw die Behandlung von Abwasser. Seine Eigenschaften Machen Sie es zu einer vielseitigen Verbindung mit eine Vielzahl der Einsatzmöglichkeiten in verschiedene Branchen.
Häufigste Fragen
Was passiert, wenn CaCl2 und Zn zusammen reagieren?
Wenn Calciumchlorid (CaCl2) und Zink (Zn) miteinander reagieren, bilden sie sich Zinkchlorid (ZnCl2) und Kalzium (Ca). Die Reaktion ist eine Verdrängungsreaktion wobei Zink Kalzium aus Kalziumchlorid verdrängt.
Was sind die drei physikalischen Eigenschaften von Calciumchlorid (CaCl2)?
Die Drei physikalische Eigenschaften von Calciumchlorid sind: es ist ein weißer Kristall Es ist bei Raumtemperatur fest, in Wasser gut löslich und hat eine hohe Löslichkeit Schmelzpunkt von 772 °C.
Wie kann eine CaCl2-Lösung hergestellt werden?
Eine CaCl2-Lösung kann durch Auflösen hergestellt werden festes Calciumchlorid in destilliertem Wasser. Die Summe Die Menge des verwendeten CaCl2 hängt davon ab die gewünschte Konzentration of die Lösung.
Warum lautet die Formel für Calciumchlorid CaCl2 und nicht CaCl?
Die Formel denn Calciumchlorid ist CaCl2 und nicht CaCl, weil Calcium (Ca) vorhanden ist eine Ladung von +2 und Chlorid (Cl) hat eine Gebühr von -1. Ausbalancieren die Gebühren, XNUMX Chloridionen werden benötigt für jedes Calciumion, daher die Formel CaCl2.
Welche Ionen entstehen, wenn CaCl2 in Wasser gelöst wird?
Wenn CaCl2 in Wasser gelöst wird, dissoziiert es in seine Ionen, wodurch Ca2+ entsteht (Kalziumionen) und 2Cl- (Chloridionen).
Welche Eigenschaften hat Calciumchlorid?
Calciumchlorid (CaCl2) ist ein weißer Kristall Feststoff, der in Wasser gut löslich ist. Es hat ein Hoch Schmelzpunkt (772°C) und Siedepunkt (1935°C). An die chemische Seite, es ist ein starker Elektrolyt und kann mit Basen und Carbonaten reagieren.
Welche Eigenschaften hat Eisen(II)-chlorid (FeCl2)?
Eisen(II)-chlorid (FeCl2) ist ein gelblich-brauner Kristall solide. Es ist in Wasser, Alkohol und Aceton löslich. Es hat ein Schmelzpunkt von 677°C und a Siedepunkt von 1023°C. Es wird in verschiedenen Anwendungen eingesetzt, z Wasseraufbereitung und in der Synthese von Eisenkomplexe.
Wie kann die Wahrscheinlichkeit berechnet werden?
Die Wahrscheinlichkeit kann mit berechnet werden statistische Methoden. in die einfachsten Begriffe, es ist Die Wahrscheinlichkeit des Beobachtens die Daten gegeben ein bestimmtes Modell. Es wird oft in verwendet der Kontext of Maximum-Likelihood-Schätzung (MLE), wo das Ziel ist zu finden die Modellparameter das maximiert die Wahrscheinlichkeitsfunktion.
Welche Vorsichtsmaßnahmen sind beim Umgang mit FeCl2 zu beachten?
FeCl2 kann beim Verschlucken oder Einatmen gesundheitsschädlich sein und Haut- und Augenreizungen verursachen. Daher sollte vorsichtig damit umgegangen werden. Trage immer entsprechende Schutzkleidung, Handschuhe u Augen-/Gesichtsschutz. Im Falle von zufälliger Kontakt, sofort mit viel Wasser abspülen.
Wozu dient Eisen(II)-chlorid (FeCl2)?
Eisen(II)-chlorid wird verwendet in eine Auswahl von Anwendungen. Es wird verwendet in Wasseraufbereitung Prozesse zur Entfernung von Verunreinigungen. Es wird auch bei der Synthese von verwendet Eisenkomplexe und als Reduktionsmittel in organische Synthese.
Nguồn: https://thuvienhaichau.edu.vn
Danh mục: Hóa