Al là gì?
Nhôm (Al) là một nguyên tố hóa học trong bảng tuần hoàn có ký hiệu “Al” và số nguyên tử 13. Nó là một kim loại nhẹ, mềm dẻo, có màu bạc và có ứng dụng rộng rãi trong nhiều lĩnh vực do tính chất dẻo dai, dẫn điện và khả năng chống ăn mòn của nó. Nhôm thường được tìm thấy trong môi trường tự nhiên dưới dạng quặng bauxite.
Cl2 là gì?
Cl2 là công thức hóa học cho khí clo. Khí clo là một phân tử hai nguyên tử của nguyên tố clo (Cl), và nó xuất hiện dưới dạng một khí màu vàng xanh, có mùi khá đặc trưng. Clo là một nguyên tố halogen trong bảng tuần hoàn và có số nguyên tử 17. Khí clo có tính chất oxi hóa mạnh và có thể tham gia vào nhiều phản ứng hóa học, bao gồm việc tác động lên kim loại để tạo ra các muối clorua.
Bạn đang xem: Phản ứng Al + Cl2 tạo ra gì? Ví dụ minh hoạ
Phản ứng Al + Cl2 là gì?
Phản ứng Al + Cl2 là phản ứng hóa học giữa nhôm (Al) và khí clo (Cl2). Phản ứng này tạo ra muối clorua nhôm, được biểu diễn bằng phương trình hóa học:
2Al + 3Cl2 → 2AlCl3
Trong phản ứng này, nhôm tác dụng với khí clo và tạo ra muối clorua nhôm (AlCl3). Đây là một ví dụ về phản ứng oxi hóa-khử, trong đó nhôm bị oxi hóa từ trạng thái số oxi hoá 0 lên +3, còn khí clo bị khử từ trạng thái số oxi hoá 0 xuống -1 trong axit clorhydric (HCl).
Phản ứng Al + Cl2 ra AlCl3 thuộc loại phản ứng oxi hóa khử, phản ứng hóa hợp đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về Al có lời giải, mời các bạn đón xem:
2Al + 3Cl2 → 2AlCl3

1. Phương trình hoá học của phản ứng Al tác dụng với Cl2
2Al + 3Cl2 → 2AlCl3
2. Nhẩm cân bằng phản ứng hoá học
– Viết sơ đồ phản ứng: Al + Cl2 −−−→”>−−−→−−−→ AlCl3.
– Làm chẵn số Cl vế phải bằng thêm hệ số 2 trước AlCl3:
Al + Cl2 −−−→”>−−−→−−−→2AlCl3
– Cân bằng số nguyên tử Al ở 2 vế bằng cách thêm hệ số 2 trước Al:
2Al + Cl2 −−−→”>−−−→−−−→2AlCl3
– Cân bằng số nguyên tử Cl ở 2 vế bằng cách thêm hệ số 3 trước Cl2:
2Al + 3Cl2 −−−→”>−−−→−−−→2AlCl3
– Kiểm tra và hoàn thiện phương trình hoá học: 2Al + 3Cl2 → 2AlCl3
3. Lập phương trình hoá học của phản ứng theo phương pháp thăng bằng electron
Trước hết, ta cần xác định các nguyên tử có sự thay đổi số oxi hoá để xác định chất oxi hoá và chất khử trong phản ứng:
Bước 1: Xác định chất oxi hoá và chất khử
Phương trình ban đầu: Al⁰ + Cl₂ → Al³⁺ + Cl⁻
Trong đó, nguyên tử nhôm (Al) đã tăng số oxi hoá từ 0 lên +3, và nguyên tử clo (Cl) đã giảm số oxi hoá từ 0 xuống -1. Do đó:
Chất oxi hoá: Cl₂Chất khử: Al⁰
Bước 2: Biểu diễn quá trình oxi hoá và quá trình khử
Quá trình oxi hoá: Cl₂ + 2e⁻ → 2Cl⁻Quá trình khử: Al⁰ → Al³⁺ + 3e⁻
Bước 3: Xác định hệ số thích hợp
Để cân bằng sự thay đổi số oxi hoá, ta nhân đôi quá trình oxi hoá và nhân ba quá trình khử:
3Cl₂ + 6e⁻ → 6Cl⁻2Al⁰ → 2Al³⁺ + 6e⁻
Bước 4: Lập phương trình hoá học và kiểm tra cân bằng nguyên tử
Phương trình hoá học đã cân bằng: 2Al + 3Cl₂ → 2AlCl₃
Thông qua quá trình trên, chúng ta có thể xác định phương trình hoá học cân bằng cho phản ứng giữa nhôm và khí clo:
2Al + 3Cl₂ → 2AlCl₃
4. Điều kiện để Al tác dụng với Cl2
Phản ứng giữa nhôm và Cl2 diễn ra ngay điều kiện thường.
Phản ứng diễn ra nhanh ở nhiệt độ cao.
5. Cách tiến hành thí nghiệm
Cho dây nhôm được đun nóng đỏ vào trong lọ chứa khí clo.
6. Hiện tượng phản ứng
Dây nhôm cháy với ngọn lửa sáng chói.
7. Tính chất hóa học của nhôm
7.1. Tác dụng với oxi và một số phi kim
– Ở điều kiện thường, nhôm phản ứng với oxi tạo thành lớp Al2O3 mỏng bền vững, lớp oxit này bảo vệ đồ vật bằng nhôm, không cho nhôm tác dụng oxi trong không khí, nước.
4Al + 3O2→ 2Al2O3
– Bột nhôm bốc cháy khi tiếp xúc với khí clo.
2Al + 3Cl2 → 2AlCl3
7.2. Nhôm tác dụng với axit
– Tác dụng với axit (HCl, H2SO4 loãng,..) giải phóng khí H2.
2Al + 6HCl → 2AlCl3 + 3H2
2Al + 3H2SO4 (loãng) → Al2(SO4)3 + 3H2
– Tác dụng với axit có tính oxi hóa mạnh như HNO3 hoặc H2SO4 đậm đặc …
Al + 4HNO3 (loãng) → Al(NO3)3 + NO + 2H2O
Al + 6HNO3 (đặc) → Al(NO3)3 + 3NO2 + 3H2O
2Al + 6H2SO4 (đặc) → Al2(SO4)3 + 3SO2 + 6H2O
Chú ý: Nhôm không tác dụng với H2SO4 (đặc, nguội), HNO3 (đặc, nguội).
7.3. Tác dụng với dung dịch muối của kim loại yếu hơn.
Nhôm có thể tác dụng với dung dịch muối của kim loại yếu hơn để tạo thành muối mới và kim loại mới (đẩy kim loại yếu hơn ra khỏi muối).
Al + 3AgNO3 → Al(NO3)3 + 3Ag
2Al + 3FeSO4 → Al2(SO4)3 + 3Fe
7.4. Tính chất hóa học riêng của nhôm
Al2O3 là oxit lưỡng tính nên lớp màng mỏng Al2O3 trên bề mặt nhôm tác dụng với dung dịch kiềm tạo ra muối tan. Khi không còn màng oxit bảo vệ, nhôm sẽ tác dụng được với nước tạo ra Al(OH)3 và giải phóng H2; Al(OH)3 là hiđroxit lưỡng tính nên tác dụng trực tiếp với kiềm.
Phản ứng nhôm tác dụng với dung dịch kiềm được thể hiện đơn giản như sau:
2Al + 2H2O + 2NaOH → 2NaAlO2+ 3H2↑
7.5. Phản ứng nhiệt nhôm
Phản ứng nhiệt nhôm là phản ứng hóa học toả nhiệt trong đó nhôm là chất khử ở nhiệt độ cao. Ví dụ nổi bật nhất là phản ứng nhiệt nhôm giữa sắt(III) oxit và nhôm:
Fe2O3 + 2Al → 2Fe + Al2O3
Nhiệt lượng do phản ứng toả ra lớn làm sắt nóng chảy nên phản ứng này được dùng để điều chế một lượng nhỏ sắt nóng chảy khi hàn đường ray.
Một số phản ứng khác như:
3CuO + 2Al → Al2O3 + 3Cu
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
Cr2O3 + 2Al → Al2O3 + 2Cr
8. Tính chất hoá học của clo (Cl2)
– Nguyên tử clo có độ âm điện lớn (3,16) chỉ sau F (3,98) và O (3,44). Vì vậy trong các hợp chất với các nguyên tố này clo có số oxi hóa dương (+1; +3; +5; +7), còn trong các trường hợp khác clo có số oxi hóa âm (-1).
– Khi tham gia phản ứng hóa học clo dễ dàng nhận thêm 1 electron:
Cl + 1e → Cl-
⇒ Tính chất hóa học cơ bản của clo là tính oxi hóa mạnh.
8.1. Tác dụng với kim loại
Khí clo có khả năng oxi hóa trực tiếp hầu hết các kim loại, tạo thành các muối clorua. Phản ứng này có thể xảy ra ở nhiệt độ thường hoặc không cần quá cao, và thường diễn ra một cách nhanh chóng, kèm theo sự tỏa nhiệt.
Dưới đây là một số ví dụ về phản ứng oxi hóa giữa khí clo và các kim loại:
– Phản ứng với natri (Na):2Na + Cl2 → 2NaCl
– Phản ứng với sắt (Fe):2Fe + 3Cl2 → 2FeCl3
– Phản ứng với đồng (Cu):Cu + Cl2 → CuCl2
Trong các phản ứng trên, khí clo thể hiện tính chất oxi hóa khi tác động lên các kim loại, góp phần trong việc chuyển đổi các kim loại thành muối clorua tương ứng.
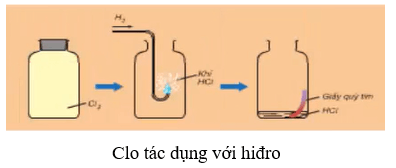
8.2. Tác dụng với hiđro
Tại nhiệt độ phòng và trong điều kiện không có ánh sáng, khí clo thường không phản ứng với khí hiđro.
Tuy nhiên, khi hỗn hợp của hai khí này được chiếu sáng bởi ánh sáng mặt trời hoặc ánh sáng của đèn cháy, phản ứng có thể xảy ra và thậm chí có khả năng gây nổ. Phản ứng nổ mạnh nhất xảy ra khi tỉ lệ số mol giữa khí hiđro và khí clo là 1:1.
Phản ứng hóa học giữa hai khí có thể được biểu diễn bằng phương trình:
H2 + Cl2 → 2HCl
Trong phản ứng này, khí clo thể hiện tính chất oxi hóa khi oxi hóa khí hiđro (H2) thành axit clohiđric (HCl).
8.3. Tác dụng với nước
Hơn nữa, khi clo tan trong nước, một phần khí clo sẽ tác dụng với nước tạo ra một hỗn hợp gồm axit clohiđric và axit hipoclozơ.
Phản ứng hóa học có thể được biểu diễn bằng phương trình:
Cl2 + H2O ⇄ HCl + HClO
Trong phản ứng này, clo tham gia cùng lúc cả quá trình oxi hóa và khử.
Phản ứng trên là một phản ứng thuận nghịch, và điều này bởi vì axit hipoclozơ (HClO) là chất oxi hóa mạnh, có khả năng oxi hóa axit clohiđric (HCl) thành khí clo (Cl2) và nước (H2O). Do axit hipoclozơ cũng có tính oxi hóa mạnh, nên nước clo cũng thể hiện tính chất tẩy màu mạnh mẽ.
Chú ý: Trong hỗn hợp nước clo, có sự hiện diện của các chất gồm Cl2, HCl, HClO và H2O.
Mở rộng:
Hơn nữa, clo còn có khả năng tham gia vào một số phản ứng hóa học khác, ví dụ như:
– Tác dụng với dung dịch bazơ:
Cl2 + 2NaOH → NaCl + NaClO + H2O
3Cl2 + 6KOH → KClO3 + 5KCl + 3H2O
– Tác dụng với muối của các halogen khác:
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
– Tác dụng với các chất khử khác:
3Cl2 + 2NH3 → N2 + 6HCl
Cl2 + SO2 + 2H2O → H2SO4 + 2HCl
Những phản ứng này cho thấy tính tương thích và đa dạng của clo trong các quá trình hóa học.
9. Bài tập vận dụng liên quan
Câu 1: Khí Cl2 ẩm có tính tẩy màu là do
A. Cl2 có tính oxi hóa mạnh.
B. Cl2 tác dụng với nước tạo thành HClO có tính tẩy màu.
C. Cl2 tác dụng với nước tạo thành dung dịch axit.
D. Cl2 vừa có tính oxi hóa, vừa có tính khử.
Hướng dẫn giải:
Chọn B
Khi hoà tan trong nước, một phần khí clo sẽ tác dụng với nước theo phản ứng thuận nghịch:
Cl2 + H2O ⇄ HCl + HClO
Axit hipoclorơ có khả năng oxi hóa mạnh mẽ, có khả năng phá hủy các chất màu. Do đó, clo ẩm có khả năng tác dụng làm mất màu.
Câu 2: Đốt 28 gam bột sắt trong khí clo dư. Khối lượng muối clorua sinh ra là
A. 32,50 gam
B. 24,50 gam
C. 81,25 gam
D. 25,40 gam
Hướng dẫn giải:
Đáp án C
Ta có: nFe = 0,5 mol
→ nFeCl3 = 0,5 mol → mFeCl3 = 81,25 gam
Câu 3:Cho 10,8 gam kim loại M tác dụng hoàn toàn với khí Cl2 dư thu được 53,4 gam muối clorua. Kim loại M là
A. Mg
B. Al
C. Fe
D. Zn
Hướng dẫn giải:
Đáp án B
M+n2Cl2→MCln
→10,8M=53,4M+35,5n→M=9n
Với n = 3 → M = 27 (Al).
Câu 4: Hiện tượng xảy ra khi cho dây sắt nóng đỏ vào bình đựng khí clo là:
A. Có khói trắng
B. Có khói nâu
C. Có khói đen
D. Có khói tím
Hướng dẫn giải:
Đáp án B
2Fe + 3Cl2 → 2FeCl3 (có màu nâu)
Câu 5. Đốt cháy hết 13,6g hỗn hợp Mg, Fe trong bình kín chứa khí clo dư, sau phản ứng thì lượng clo trong bình giảm tương ứng 0,4 mol. Khối lượng muối clorua khan thu được là.
A. 65,0 g. B. 38,0 g. C. 50,8 g. D. 42,0 g.
Hướng dẫn giải
Đáp án D
mmuối = mKL+mCl2=13,6+0,4×71=42
Câu 6. Đun nóng Na với Cl2 thu được 11,7 gam muối. Khối lượng Na và thể tích khí clo (đktc) đã phản ứng là
A. 4,6gam; 2,24 lít. B. 2,3gam; 2,24 lít.
C. 4,6gam; 4,48lít. D. 2,3gam; 4,48 lít.
Hướng dẫn giải
Đáp án A
2Na + Cl2 → 2 NaCl
0,2 0,1 0,2 (mol).
Khối lượng Na là: 23 . 0,2 = 4,6g.
Thể tích Cl2: 0,1 . 22,4= 2,24 lít.
Câu 7. Cho clo tác dụng với vừa đủ với Fe rồi hòa tan lượng muối sinh ra vào nước được 100g dung dịch muối có nồng độ 16,25%. Khối lượng sắt và clo (đktc) đã dùng là
A. 0,56 gam; 2,24 lít
B. 5,6 gam; 3,36 lít
C. 11,2 gam; 4,48 lít
D. 1,12 gam; 2,4 lít
Hướng dẫn giải
Đáp án B
– Từ khối lượng FeCl3 đã cho: mFeCl3 = 16.25 g, ta suy ra nFeCl3 = 0.1 mol.
– Sử dụng phép tính, ta thấy rằng khối lượng sắt (Fe) cần là: mFe = 0.1 mol × 56 g/mol = 5.6 g.
– Theo phương trình phản ứng 2Fe + 3Cl2 → 2FeCl3, cho 0.1 mol FeCl3, ta sử dụng 0.1 mol Fe và 0.15 mol Cl2.
– Dựa vào khối lượng của Fe và số mol Cl2, ta tính được thể tích clo (Cl2) đã sử dụng: V = 0.15 mol × 22.4 L/mol = 3.36 L.
Như vậy, sau phản ứng, sẽ thu được 16.25 g FeCl3, đã sử dụng 5.6 g sắt (Fe) và 3.36 lít khí clo (Cl2).
Câu 8. Cho 14 gam Fe vào bình chứa 10,08 lít clo (đktc) tác dụng với nung nóng rồi lấy chất rắn thu được hoà vào nước và khuấy đều thì thu được 500 g dung dịch X. Nồng độ phần trăm của dung dịch X là
A. 6,35% B. 9,19% C. 8,125% D. 11,43%
Hướng dẫn giải
Đáp án C
Phản ứng hóa học đã cho:
2Fe + 3Cl2 → 2FeCl3
Số mol ban đầu của Fe và Cl2 lần lượt là: 0,25 mol và 0,45 mol.
Sau phản ứng, số mol của Cl2 đã phản ứng là 0,375 mol (theo tỉ lệ 2:3 với Fe).
Số mol Cl2 còn lại sau phản ứng: 0,45 mol – 0,375 mol = 0,075 mol.
Vì số mol Cl2 còn lại lớn hơn 0, nên Clo là chất dư trong phản ứng.
Khối lượng muối FeCl3 thu được được tính bằng khối lượng mol và số mol tương ứng:
m = n * M = 0,25 mol * 162,5 g/mol = 40,625 g
Từ đó, tính được tỷ lệ phần trăm khối lượng muối trong hỗn hợp ban đầu:
C% = (40,625 g / 500 g) * 100% = 8,125%
Vậy, khối lượng muối thu được là 40,625 g và tỷ lệ phần trăm khối lượng muối trong hỗn hợp ban đầu là 8,125%.
Câu 9. Cho 0,12 mol Al tác dụng vừa hết với đơn chất halogen X2 thu được 16,02 gam muối Y. Cho các phát biểu sau
(1) X thuộc chu kì 3, nhóm VIIA trong bảng HTTH.
(2) X oxi hóa Fe thành muối Fe2+ ở nhiệt độ cao.
(3) X là nguyên tố có độ âm điện lớn nhất trong nhóm halogen.
(4) Phản ứng giữa X2 và H2 gây nổ mạnh ở tỉ lệ thể tích 1:1.
(5) Dung dịch NaX không tác dụng với dung dịch AgNO3 dư.
(6) Muối NaXO được dùng để tẩy rửa.
(7) Điện phân dung dịch là phương pháp duy nhất để điều chế X2.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 6.
Hướng dẫn giải
Đáp án A
Phản ứng đã cho:
2Al + 3X2 → 2AlX3
Cho 0,12 mol hỗn hợp Al và X2 phản ứng, thu được 0,18 mol hỗn hợp sản phẩm AlX3.
Dựa vào phương trình phản ứng, ta có:
0,12 mol Al tác dụng với 0,18 mol X2 tạo thành 0,18 mol AlX3.
Từ đó, ta có phương trình quy đổi số mol:
0,12. (27 + 3MX) = 16,02
Trong đó, 27 là khối lượng mol của 1 mol Al, và MX là khối lượng mol của 1 mol X.
Tính toán ta được:
MX = 35,5 ⇒ X là Clo
Vậy, những phát biểu (1), (4) và (6) là đúng.
Câu 10. Cho m gam bột Fe tác dụng với khí Cl2 sau khi phản ứng kết thúc thu được m + 12,78 gam hỗn hợp X. Hoà tan hết hỗn hợp X trong nước cho đến khi X tan tối đa thì thuđược dung dịch Y và 1,12 gam chất rắn. Giá trị của m là.
A. 5,6 gam B. 11,2 gam C. 16,8 gam D. 8,4 gam.
Hướng dẫn giải
Đáp án B
Trong phản ứng hóa học giữa 2 mol sắt (Fe) và 3 mol khí clo (Cl2), ta thu được 2 mol FeCl3:
2Fe + 3Cl2 → 2FeCl3
Nhưng trong phản ứng ngược lại, 1 mol sắt (Fe) tác dụng với 2 mol FeCl3 để tạo thành 3 mol FeCl2:
Fe + 2FeCl3 → 3FeCl2
Từ đó, ta có thể suy ra tỷ lệ số mol giữa sắt và clo trong phản ứng:
nFe pư = nClo
Từ công thức tính toán, ta có:
m − 1,1256 = 12,7871
Vậy khối lượng của mẫu chứa sắt là:
m = 11,2g
Câu 11. Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là.
A. 75,68%. B. 24,32%. C. 51,35%. D. 48,65%.
Hướng dẫn giải
Đáp án B
Đặt lượng mol khí Cl2 là x mol; lượng mol khí O2 là y mol. Dựa theo vấn đề đã cho, chúng ta có hệ phương trình sau:
x + y = 7,842,47x + 32y = 30,1 – 11,1 = 19⇔ x = 0,2, y = 0,15
Khi gọi lượng mol của Mg và Al lần lượt là a và b mol, chúng ta cũng có hệ phương trình sau:
24a + 27b = 11,12a + 3b = 0,2 * 2 + 0,15 * 4⇔ a = 0,35, b = 0,1
Từ đó, ta tính được tỷ lệ phần trăm của Al trong hợp chất:
%mAl = 0,1 / 2 * 11,1 * 100% = 24,32%.
Câu 12:Kim loại Al không phản ứng với dung dịch
A.HNO3 đặc, nguội. B. Cu(NO3)2.
C.HCl. D. KOH.
Hướng dẫn giải
Đáp án A
Al không phản ứng với HNO3 đặc, nguội, H2SO4 đặc nguội
Xem thêm các phương trình hóa học hay khác:
- 4Al + 3O2 → 2Al2O3
- 2Al + 3S → Al2S3
- 2Al + 6HCl → 2AlCl3 + 3H2
- 2Al + 3H2SO4(loãng) → Al2(SO4)3 + 3H2
- 2Al + 6H2SO4(đặc) → Al2(SO4)3 + 3SO2 ↑ + 6H2O.
- 8Al + 30HNO3(loãng) → 8Al(NO3)3 + 3NH4NO3 + 9H2O
- Al + 6HNO3(đặc, nóng) → Al(NO3)3 + 3NO2 + 3H2O
- 2Al + Fe2O3 → Al2O3 + 2Fe
- 2Al + 6H2O → 2Al(OH)3 ↓ + 3H2 ↑
- Phản ứng hóa học:2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
- 2Al + 3Br2 → 2AlBr3
- 2Al + 3I2 → 2AlI3
- 2Al + 3F2 → 2AlF3
- 4Al + 3C → Al4C3
- 2Al + 2NH3 → 2AlN + 3H2 ↑
- 4Al + 3CO2 → 2Al2O3 + 3C
- 2Al + 3CuO → Al2O3 + 3Cu
- 2Al + 3CuCl2 → 2AlCl3 + 3Cu
- 2Al + 3Cu(NO3)2 → 3Cu + 2Al(NO3)3
- 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
- 2Al + 3FeO → Al2O3 + 3Fe
- 8Al + 3Fe3O4 → 4Al2O3 + 9Fe
- 2Al + 3FeCl2 → 2AlCl3 + 3Fe
- Al + 3FeCl3 → AlCl3 + 3FeCl2
- Al + FeCl3 → AlCl3 + Fe
- 2Al + 3FeSO4 → Al2(SO4)3 + 3Fe
- Al + Fe2(SO4)3 → Al2(SO4)3 + FeSO4
- 2Al + 3Fe(NO3)2 → 3Fe + Al(NO3)3
- Al + 3Fe(NO3)3 → 3Fe(NO3)2 + Al(NO3)3
- 2Al + Cr2O3 → Al2O3 + 2Cr
- 2Al + Cr2(SO4)3 → Al2(SO4)3 + 2Cr
- 2Al + 3PbO → Al2O3 + 3Pb
- 2Al + 3SnO → Al2O3 + 3Sn
- 8Al + 3Mn3O4 → 4Al2O3 + 9Mn
- Al + 3AgNO3 → 3Ag + Al(NO3)3
- 2Al + 3ZnSO4 → Al2(SO4)3 + 3Zn
- 2Al + 3Pb(NO3)2 → 2Al(NO3)3 + 3Pb
- 4Al + 3SiO2 → 2Al2O3 + 3Si
- 2Al + 3CaO → Al2O3 + 3Ca
- 10Al + 6NH4ClO4 → 5Al2O3 + 9H2O + 6HCl + 3N2 ↑
- 8Al + 3KClO4 → 4Al2O3 + 3KCl
- 2Al + 4H2SO4 → Al2(SO4)3 + 4H2O + S ↓
- 8Al + 15H2SO4 → 4Al2(SO4)3 + 12H2O + 3H2S ↑
- 8Al + 27HNO3 → 9H2O + 3NH3 ↑ + 8Al(NO3)3
- Al + 4HNO3 → 2H2O + NO ↑ + Al(NO3)3
- 10Al + 36HNO3 → 18H2O + 3N2 ↑ + 10Al(NO3)3
- 2Al + 6HF → 3H2 ↑ + 2AlF3
- 2Al + 3H2S → Al2S3 + 3H2 ↑
- 2Al + 6CH3COOH → 2(CH3COO)3Al + 3H2 ↑
- 2Al + 2H3PO4 → 3H2 ↑ + 2AlPO4
- 2Al + 6HBr → 3H2 ↑ + 2AlBr3
- 4Al + K2Cr2O7 → Al2O3 + 2Cr + 2KAlO2
- 8Al + 21H2SO4 + 3K2Cr2O7 → 4Al2(SO4)3 + 21H2O + 3K2SO4 + 6CrSO4
- 2Al + 3H2O → Al2O3 + 3H2 ↑
- Al + 6KNO3 → 2Al2O3 + 3N2 ↑ + 6KAlO2
- 8Al + 2H2O + 3NaNO3 + 5NaOH → 3NH3 ↑ + 8NaAlO2
- 8Al + 18H2O + 3KNO3 + 5KOH → 3NH3 ↑ + 8KAl(OH)4
- 2Al + 4BaO → 3Ba + Ba(AlO2)2
- 2Al + 4CaO → 3Ca + Ca(AlO2)2
- Al + Ca(OH)2 + H2O → H2 ↑ + Ca(AlO2)2
- 2Al + 2H2O + Ba(OH)2 → 3H2 ↑ + Ba(AlO2)2
- 2Al + 2H2O + 2KOH → 3H2 ↑ + 2KAlO2
- 2Al + 2H2O + 2NaOH → 3H2 ↑ + 2NaAlO2
10. Mọi người cũng hỏi
Phản ứng Al + Cl2 tạo ra sản phẩm gì?
Trả lời: Phản ứng giữa nhôm (Al) và clo (Cl2) tạo ra sản phẩm là muối nhôm clo (AlCl3). Công thức phản ứng là: 2Al + 3Cl2 → 2AlCl3.
Điều gì xảy ra trong quá trình phản ứng giữa Al và Cl2?
Trả lời: Trong quá trình phản ứng, nhôm (Al) tác dụng với clo (Cl2), mỗi nguyên tử nhôm tương tác với ba phân tử clo. Nhôm sẽ mất đi hai electron để trở thành ion nhôm Al3+, trong khi clo sẽ nhận thêm electron để trở thành ion clo Cl-. Khi hai ion Al3+ kết hợp với sáu ion Cl-, ta thu được muối nhôm clo AlCl3.
Tính chất của muối nhôm clo (AlCl3) là gì?
Trả lời: Muối nhôm clo (AlCl3) là một chất rắn, màu trắng hoặc màu vàng nhạt, có cấu trúc tinh thể và hút ẩm mạnh. Nó hòa tan tốt trong nước, tạo ra dung dịch có tính axit mạnh và thường được sử dụng trong các ứng dụng công nghiệp như chất xúc tác và chất điều chỉnh.
Phản ứng Al + Cl2 có ứng dụng gì trong thực tế?
Trả lời: Phản ứng giữa nhôm và clo có nhiều ứng dụng trong thực tế. Muối nhôm clo (AlCl3) được sử dụng trong sản xuất nhựa và cao su, trong quá trình tạo ester và amin từ cồn và amin, và trong các quá trình trao đổi proton. Ngoài ra, nó cũng được dùng trong công nghệ hóa dầu và sản xuất thuốc nhuộm và mỹ phẩm.
Nguồn: https://thuvienhaichau.edu.vn
Danh mục: Hóa